Onderzoekers van de Vrije Universiteit Brussel onder leiding van Prof. Dr. Eline Menu hebben onderzocht hoe veranderingen in de stofwisseling bijdragen aan kankerresistentie en herval. Zij identificeerden het aminozuur proline als een belangrijke voedingsbron voor de groei van kwaadaardige plasmacellen, het kenmerkende fenomeen bij myeloom. Hun bekroonde onderzoek, uitgevoerd door doctoraatstudente Inge Oudaert, toont een nieuwe mogelijke behandelingsstrategie in de zoektocht naar kankergenezing.
Multipel Myeloom, ook wel de ziekte van Kahler genoemd, is een bloedkanker waarbij een ongecontroleerde groei van plasmacellen plaatsvindt in het beenmerg. Deze grote hoeveelheid aan abnormale kankercellen neemt de plaats in van andere celtypes, zoals rode bloedcellen, bloedplaatjes, normale witte bloedcellen, waardoor ook hun functies belemmerd worden. Hierdoor hebben patiënten vaak te maken met bloedarmoede, blauwe plekken en een langere bloedingstijd, alsook een verhoogd risico op infecties. Elk jaar krijgen zo’n 1000 patiënten in België te horen dat ze lijden aan multipel myeloom. Zo’n 40% hiervan zal binnen de vijf jaar overlijden.
Ongeneeslijke ziekte
De onderzoeksgroep Hematologie en Immunologie, die deel uitmaakt van het Oncology Research Center (orc.vub.be) aan de Vrije Universiteit Brussel voert reeds jaren succesvol onderzoek uit naar deze bloedkanker. Omdat deze ziekte nog altijd ongeneeslijk is, blijven deze onderzoekers zich tot het uiterste inzetten om de ontwikkeling en progressie van deze ziekte verder uit te spitten en nieuwe behandelingsmethoden uit te testen.
Ontdekking rol proline
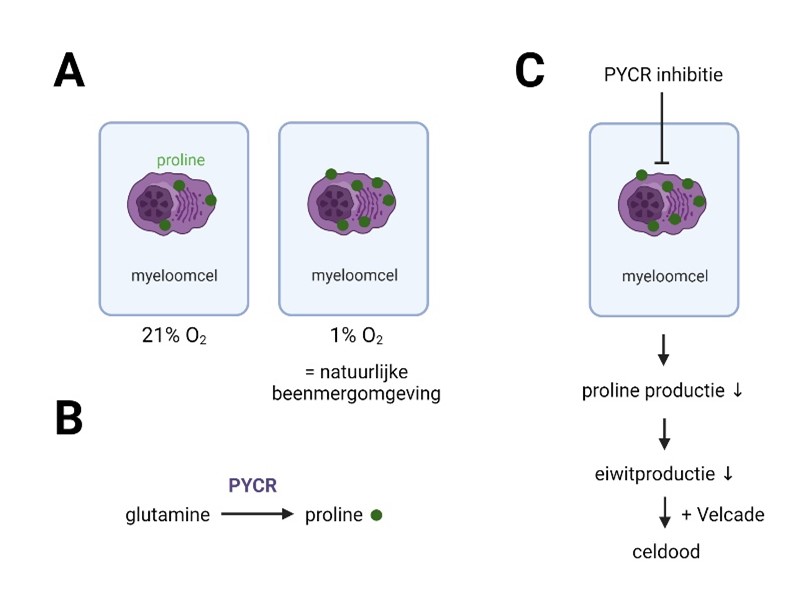
De voorbije drie jaar heeft het onderzoeksteam zich verder toegespitst op welke voedingsstoffen deze kankercellen nodig hebben om te kunnen blijven groeien. Één van deze voedingstoffen bleek proline te zijn, een aminozuur nodig voor eiwitproductie, maar ook voor de DNA/RNA productie, de verwijdering van toxische stoffen uit het lichaam en de productie van energie. Een initieel experiment toonde aan dat myeloomcellen meer glutamine naar proline omzetten wanneer zij gekweekt worden in een zuurstofarme omgeving, een typisch kenmerk van de natuurlijke beenmergomgeving. Ook de proline productie zelf was verhoogd in een zuurstofarme omgeving. Verder vertoonden myeloom patiënten in herval ook hogere expressie van het PYCR gen, dat verantwoordelijk is voor proline productie.
Eerste testen
Om te kijken of proline inhibitie een goede behandelingsmethode zou zijn, werden kankercellen in het labo behandeld met een PYCR inhibitor, alsook de PYCR genexpressie geblokkeerd met behulp van klein interfererend RNA. PYCR inhibitie verminderde de leefbaarheid en de vermenigvuldiging van de kankercellen, en veroorzaakte ook celdood van de kankercellen. Verder onderzoek naar de onderliggende veranderingen toonden aan dat het PYCR gen belangrijk is voor eiwit, DNA en RNA productie en dat PYCR inhibitie deze processen verminderden, leidend tot een vertraagde cel groei van de kankercellen en uiteindelijk ook hun celdood.
Beloftevolle resultaten
Myeloompatiënten worden momenteel behandeld met een combinatietherapie bestaande uit meerdere geneesmiddelen waaronder Velcade. Om te evalueren of PYCR inhibitie hier ook deel van zou kunnen uitmaken, werden myeloomcellen gelijktijdig behandeld met Velcade en de PYCR inhibitie. Hierbij bleek dat de combinatietherapie meer celdood van kankercellen induceerde vergeleken met de individuele therapieën. Deze combinatietherapie werd ook getest op zieke myeloom-dragende muizen, waar opnieuw de combinatietherapie de ziekte beter kon afremmen.
Bekroond onderzoek
Dit onderzoek werd in december 2021 nog bekroond met de American Society of Hematology Abstract Achievement Award op het jaarlijkse hematologie congres in Atlanta, VS. Dit onderzoek werd tevens geaccepteerd voor publicatie op 7 januari 2022 en is gepubliceerd in het vooraanstaand tijdschrift ‘Journal of Experimental and Clinical Cancer Research’
